CHLOREK/B-250
ID#199400 CHLOREK/B-250
CHLOREK/B-250Категорії: Матеріали для виробниц. друкованих плат
Залізо хлорне FeCl 3 - сильно гігроскопічні, на дотик дуже схожі на мокрий пісок, іржаво-коричнево-чорні кристали, гексагональна решітка з характеристиками а = 5, 92 Å, с = 17, 26 Å; щільність становить 2, 8 г / см 3 . Температура плавлення становить 309 ° С, температура кипіння -319 ° С.
Вище 500 ° С хлорне залізо під зменшеним тиском розкладається на FeCl 2 і Cl 2 . Розчинність FeCl 3 в воді становить при 20 ° С 91, 9 гр., При 100 ° С - 537гр. Розчиняється також в спирті і ефірі, розчини яких, виставлені на сонце, знебарвлюються з випадає хлористим залізом FeCl 2 і виділяється хлор. Водний розчин хлорного заліза, якщо залишається довгий час, розкладається, виділяючи осад основної солі, що показує мінливість хлорного заліза, як і інших солей окису заліза.
У розведених розчинах хлорне залізо гідролізується до Fe (OH) 2 + , а в дуже розбавлених - до Fe (OH) + 2 . FeCl 3 утворює ряд сильно гігроскопічних кристаллогидратов, розпливаються на повітрі; з них плавляться: FeCl 3 . 6H 2 O при 37 ° С, FeCl 3 . 3, 5H 2 O при 32, 5 ° С, FeCl 3 . 2, 5H 2 O при 56 ° С, FeCl 3 . 2H 2 O при 73, 5 ° С. З розчинів можуть бути виділені основні солі - оксихлориди. FeCl 3 з солями лужних металів утворює комплекси типу Me [FeCl 4 ] і Me 3 [FeCl 6 ].
Хлорне залізо утворюється при нагріванні заліза з хлором. У великих кількостях воно виходить як побічний продукт у виробництві TiCl 4 , AlCl 3 і інші гарячим хлоруванням руд. FeCl 3 можна отримати також хлоруванням або окисленням розчину (або суспензії) FeCl 2 з подальшим випаровуванням раствораFeCl 3 до концентрації, при якій він не охолоджувався твердне у вигляді FeCl 3 . 6H 2 O.
Застосовують хлорне залізо як коагулянт при очищенні води, як протравлення для фарбування тканин, як каталізатор в органічному синтезі, а також для приготування інших солей заліза і залізних пігментів. Радіоаматори застосовують розчин хлорного заліза для травлення друкованих плат.

 Аксесуари до вентиляторів
Аксесуари до вентиляторів
 Дроти живлення
Дроти живлення
 Кожухи
Кожухи
 Вентилятори AC
Вентилятори AC
 Вентилятори AC 230V
Вентилятори AC 230V
 Вентилятори DC
Вентилятори DC
 Вентилятори DC 12В
Вентилятори DC 12В
 Вентилятори DC 24В
Вентилятори DC 24В
 Вентилятори DC 48В
Вентилятори DC 48В
 Вентилятори DC 5В
Вентилятори DC 5В
 Аксесуари для світлодіодів
Аксесуари для світлодіодів
 Блоки живлення для світлодіодів
Блоки живлення для світлодіодів
 Радіатори для світлодіодів LED
Радіатори для світлодіодів LED
 лінзи
лінзи
 патрони
патрони
 інше
інше
 Джерела світла - світлодіодні модулі
Джерела світла - світлодіодні модулі
 Джерела світла - світлодіодні стрічки
Джерела світла - світлодіодні стрічки
 Дисплеї
Дисплеї
 Дисплеї LCD
Дисплеї LCD
 Дисплеї LCD буквено-цифрові
Дисплеї LCD буквено-цифрові
 Дисплеї LED
Дисплеї LED
 Дисплеї LED матриці
Дисплеї LED матриці
 Дисплеї LED одинарні
Дисплеї LED одинарні
 Дисплеї LED подвійні
Дисплеї LED подвійні
 Дисплеї LED потрійні
Дисплеї LED потрійні
 Дисплеї LED четверні
Дисплеї LED четверні
 Ліхтарик
Ліхтарик
 Мініатюрні джерела світла
Мініатюрні джерела світла
 Оптрони
Оптрони
 Оптотріаки SMD
Оптотріаки SMD
 Оптрони логічний вихід
Оптрони логічний вихід
 Світлодіоди
Світлодіоди
 Інфрачервоні LEDи
Інфрачервоні LEDи
 Світлодіоди SMD
Світлодіоди SMD
 Світлодіоди SMD 0805
Світлодіоди SMD 0805
 Світлодіоди SMD 1206
Світлодіоди SMD 1206
 Світлодіоди SMD PLCC
Світлодіоди SMD PLCC
 Світлодіоди SMD інші
Світлодіоди SMD інші
 Світлодіоди потужності
Світлодіоди потужності
 Світлодіоди потужності 3Вт
Світлодіоди потужності 3Вт
 Світлодіоди потужності 5Вт
Світлодіоди потужності 5Вт
 Світлодіоди потужності інші
Світлодіоди потужності інші
 світлодіоди THT
світлодіоди THT
 Світлодіоди THT 12V
Світлодіоди THT 12V
 Світлодіоди THT 1.8мм
Світлодіоди THT 1.8мм
 Світлодіоди THT 10мм
Світлодіоди THT 10мм
 Світлодіоди THT 3мм
Світлодіоди THT 3мм
 Світлодіоди THT 8мм
Світлодіоди THT 8мм
 Світлодіоди THT Superflux
Світлодіоди THT Superflux
 Світлодіоди THT овальні
Світлодіоди THT овальні
 Світлодіоди THT прямокутні
Світлодіоди THT прямокутні
 Світлодіоди THT інші
Світлодіоди THT інші
 Фотоелементи
Фотоелементи
 Інтегровані інфрачервоні приймачі
Інтегровані інфрачервоні приймачі
 Фотодіоди
Фотодіоди
 Фоторезистори
Фоторезистори
 Фототранзистори
Фототранзистори
 Датчики і перетворювачі
Датчики і перетворювачі
 Датчики вологості
Датчики вологості
 Датчики магнітного поля
Датчики магнітного поля
 Датчики Холла
Датчики Холла
 Датчики магніт. поля резистивні
Датчики магніт. поля резистивні
 Контактрони
Контактрони
 Датчики рівня рідини
Датчики рівня рідини
 Датчики ультразвукові
Датчики ультразвукові
 Датчики фотооптичні
Датчики фотооптичні
 Датчики фотооптичні для друку
Датчики фотооптичні для друку
 Датчики фотооптичні стандартні
Датчики фотооптичні стандартні
 Датчики і перетворювачі температури
Датчики і перетворювачі температури
 Датчики температури - резистивні
Датчики температури - резистивні
 Датчики індукційні циліндричні
Датчики індукційні циліндричні
 Датчики індукційні прямокутні
Датчики індукційні прямокутні
 Датчики індукційні циліндричні
Датчики індукційні циліндричні
 Датчики індукційні циліндричні DC
Датчики індукційні циліндричні DC
 Термостати
Термостати
 Двигуни електричні
Двигуни електричні
 Електромагніти
Електромагніти
 Регулювання і управління
Регулювання і управління
 Вимикачі кінцеві
Вимикачі кінцеві
 Батареї, акумулятори
Батареї, акумулятори
 Акумулятори
Акумулятори
 Батареї
Батареї
 Батареї - гнізда і тримачі
Батареї - гнізда і тримачі
 Блоки живлення
Блоки живлення
 Блоки живлення від мережі
Блоки живлення від мережі
 Блоки живлення для світлодіодів
Блоки живлення для світлодіодів
 Блоки живлення промислові
Блоки живлення промислові
 Блоки живлення імпульсні відкриті
Блоки живлення імпульсні відкриті
 Зарядні пристрої до акумуляторів
Зарядні пристрої до акумуляторів
 Акустичні сигналізатори
Акустичні сигналізатори
 П'єзоперетворювачі
П'єзоперетворювачі
 Без генератора
Без генератора
 З генератором
З генератором
 Без генератора
Без генератора
 Динаміки
Динаміки
 Мікрофони і навушники
Мікрофони і навушники
 З'єднувачі аудіо, відео
З'єднувачі аудіо, відео
 Адаптери і перехідники AV
Адаптери і перехідники AV
 З'єднувачі DIN і мини-DIN
З'єднувачі DIN і мини-DIN
 З'єднувачі DIN
З'єднувачі DIN
 З'єднувачі міні-DIN
З'єднувачі міні-DIN
 З'єднувачі EURO, HDMI
З'єднувачі EURO, HDMI
 З'єднувачі Jack
З'єднувачі Jack
 З'єднувачі RCA (CINCH)
З'єднувачі RCA (CINCH)
 З'єднувачі XLR і мини-XLR
З'єднувачі XLR і мини-XLR
 З'єднувачі XLR
З'єднувачі XLR
 З'єднувачі міні-XLR
З'єднувачі міні-XLR
 З'єднувачі для динаміків
З'єднувачі для динаміків
 З'єднувачі мікрофонні
З'єднувачі мікрофонні
 З'єднувачі для передачі даних
З'єднувачі для передачі даних
 З'єднувачі Centronic
З'єднувачі Centronic
 З'єднувачі D-Sub
З'єднувачі D-Sub
 З'єднувачі RJ
З'єднувачі RJ
 З'єднувачі USB і IEEE1394
З'єднувачі USB і IEEE1394
 З'єднувачі для карт
З'єднувачі для карт
 З'єднувачі живлення
З'єднувачі живлення
 З'єднувачі AC
З'єднувачі AC
 З'єднувачі DC
З'єднувачі DC
 Планки притискні
Планки притискні
 Планки притискні для друку
Планки притискні для друку
 Роз'єми для LED
Роз'єми для LED
 Роз'єми для сонячних батарей
Роз'єми для сонячних батарей
 З'єднувачі коаксиальні/RF
З'єднувачі коаксиальні/RF
 Адаптери і перехідники RF
Адаптери і перехідники RF
 З'єднувачі BNC
З'єднувачі BNC
 З'єднувачі F
З'єднувачі F
 З'єднувачі FME
З'єднувачі FME
 З'єднувачі N
З'єднувачі N
 З'єднувачі SMA, SMB, SM
З'єднувачі SMA, SMB, SM
 З'єднувачі TNC
З'єднувачі TNC
 З'єднувачі UHF і MINI-UHF
З'єднувачі UHF і MINI-UHF
 З'єднувачі коаксиальні для антен TV
З'єднувачі коаксиальні для антен TV
 З'єднувачі промислові
З'єднувачі промислові
 З'єднувачі Automotive
З'єднувачі Automotive
 З'єднувачі круглі
З'єднувачі круглі
 З'єднувачі C091A
З'єднувачі C091A
 З'єднувачі C16-1 EcoMate
З'єднувачі C16-1 EcoMate
 З'єднувачі M8
З'єднувачі M8
 З'єднувачі WEIPU
З'єднувачі WEIPU
 З'єднувачі промислові інші
З'єднувачі промислові інші
 З'єднувачі прямокутні
З'єднувачі прямокутні
 З'єднувачі TE Connectivity
З'єднувачі TE Connectivity
 З'єднувачі сигнальні
З'єднувачі сигнальні
 З'єднувачі DIN 41.612, DIN 41.617
З'єднувачі DIN 41.612, DIN 41.617
 З'єднувачі Dubox растр 2,54мм
З'єднувачі Dubox растр 2,54мм
 З'єднувачі FFC/FPC
З'єднувачі FFC/FPC
 Стрічки FFC/FPC
Стрічки FFC/FPC
 З'єднувачі IDC
З'єднувачі IDC
 З'єднувачі сигнальні растрові
З'єднувачі сигнальні растрові
 З'єднувачі сигнальні растр 1,00мм
З'єднувачі сигнальні растр 1,00мм
 З'єднувачі сигнальні растр 1,25мм
З'єднувачі сигнальні растр 1,25мм
 З'єднувачі сигнальні растр 1,50мм
З'єднувачі сигнальні растр 1,50мм
 З'єднувачі сигнальні растр 2,00мм
З'єднувачі сигнальні растр 2,00мм
 З'єднувачі сигнальні растр 2,50мм
З'єднувачі сигнальні растр 2,50мм
 З'єднувачі сигнальні растр 2,54мм
З'єднувачі сигнальні растр 2,54мм
 З'єднувачі сигнальні растр 3,00мм
З'єднувачі сигнальні растр 3,00мм
 З'єднувачі сигнальні растр 3,96мм
З'єднувачі сигнальні растр 3,96мм
 З'єднувачі сигнальні растр 4,20мм
З'єднувачі сигнальні растр 4,20мм
 З'єднувачі сигнальні растр 4,50мм
З'єднувачі сигнальні растр 4,50мм
 З'єднувачі сигнальні растр 5,08мм
З'єднувачі сигнальні растр 5,08мм
 З'єднувачі сигнальні растр 6,35мм
З'єднувачі сигнальні растр 6,35мм
 Штекерні планки і гнізда
Штекерні планки і гнізда
 Конектори і кабельні наконечники
Конектори і кабельні наконечники
 Ізольовані конектори
Ізольовані конектори
 Затискні втулки
Затискні втулки
 Неізольовані конектори
Неізольовані конектори
 Паяльні штифти PCB
Паяльні штифти PCB
 Запобіжники - тримачі
Запобіжники - тримачі
 Запобіжники - автомобільні гнізда
Запобіжники - автомобільні гнізда
 Запобіжники - тримачі PCB
Запобіжники - тримачі PCB
 Запобіжники - тримачі для панелі
Запобіжники - тримачі для панелі
 Запобіжники - тримачі кабелів
Запобіжники - тримачі кабелів
 Запобіжники 5x20мм
Запобіжники 5x20мм
 Запобіжники 6,3x32мм
Запобіжники 6,3x32мм
 Запобіжники SMD
Запобіжники SMD
 Запобіжники SMD 0805
Запобіжники SMD 0805
 Запобіжники SMD 1206
Запобіжники SMD 1206
 Запобіжники SMD 2410
Запобіжники SMD 2410
 Запобіжники автомобільні
Запобіжники автомобільні
 Інші автомобільні запобіжники
Інші автомобільні запобіжники
 Запобіжники автомобільні міні
Запобіжники автомобільні міні
 Запобіжники автомобільні стандартні
Запобіжники автомобільні стандартні
 Запобіжники мініатюрні аксіальні
Запобіжники мініатюрні аксіальні
 Мініатюрні запобіжники TR5
Мініатюрні запобіжники TR5
 Запобіжники мініатюрні TR5 повільні
Запобіжники мініатюрні TR5 повільні
 Запобіжники полімерні РТС
Запобіжники полімерні РТС
 Запобіжники полімерні THT
Запобіжники полімерні THT
 Запобіжники термічні
Запобіжники термічні
 Переривники
Переривники
 Запобіжники високовольтні
Запобіжники високовольтні
 Корпуси для пультів
Корпуси для пультів
 Корпуси для шини DIN
Корпуси для шини DIN
 Корпуси з кріпленням
Корпуси з кріпленням
 Корпуси з панелю
Корпуси з панелю
 Корпуси панельні
Корпуси панельні
 Корпуси пристроїв сигналізац. і датчиків
Корпуси пристроїв сигналізац. і датчиків
 Корпуси універсальні
Корпуси універсальні
 Гайки
Гайки
 Гвинти
Гвинти
 Елементи дистанційні металеві
Елементи дистанційні металеві
 Елементи дистанційні пластикові
Елементи дистанційні пластикові
 Дюбелі пластмасові
Дюбелі пластмасові
 Пластмасові дистанційні втулки
Пластмасові дистанційні втулки
 Магніти
Магніти
 Ніжки і коліщатка
Ніжки і коліщатка
 Ніжки
Ніжки
 Шайби
Шайби
 Шурупи
Шурупи
 Інтегральні схеми
Інтегральні схеми
 Інтегральні логічні схеми
Інтегральні логічні схеми
 Логічні схеми сімейства CMOS
Логічні схеми сімейства CMOS
 Логічні схеми сімейства TTL
Логічні схеми сімейства TTL
 Інтегральні периферійні схеми
Інтегральні периферійні схеми
 Мультиплексори і перемикачі аналогові
Мультиплексори і перемикачі аналогові
 Перетворювачі D/A - інтегральні схеми
Перетворювачі D/A - інтегральні схеми
 Схеми watchdog і reset
Схеми watchdog і reset
 Інтеграль. схеми - інтерф. RS232/422/485
Інтеграль. схеми - інтерф. RS232/422/485
 Інтегральні схеми - інтерфейс USB
Інтегральні схеми - інтерфейс USB
 Вимикачі - інтегральні схеми
Вимикачі - інтегральні схеми
 Драйвери MOSFET/IGBT
Драйвери MOSFET/IGBT
 Драйвери для двигунів і ШІМ
Драйвери для двигунів і ШІМ
 Компаратори
Компаратори
 Операційні підсилювачі
Операційні підсилювачі
 Перетворювачі U/I, U/f, U/U
Перетворювачі U/I, U/f, U/U
 Перетворювачі температури
Перетворювачі температури
 Світлодіодні драйвери
Світлодіодні драйвери
 Мікроконтролери
Мікроконтролери
 Мікроконтролери Atmel
Мікроконтролери Atmel
 Мікроконтролери Atmel 8051 SMD
Мікроконтролери Atmel 8051 SMD
 Мікроконтролери Atmel 8051 THT
Мікроконтролери Atmel 8051 THT
 Мікроконтролери Atmel AVR SMD
Мікроконтролери Atmel AVR SMD
 Мікроконтролери ST
Мікроконтролери ST
 Мікроконтролери інші
Мікроконтролери інші
 Пам'ять - інтегральні схеми
Пам'ять - інтегральні схеми
 Пристр. пам'яті FLASH - інтеграль. схеми
Пристр. пам'яті FLASH - інтеграль. схеми
 Пристрої пам'яті FRAM - інтеграль. схеми
Пристрої пам'яті FRAM - інтеграль. схеми
 Джерела напруги віднесення - схеми
Джерела напруги віднесення - схеми
 Лінійні стабілізатори - інтегральні схем
Лінійні стабілізатори - інтегральні схем
 Стабілізатори напруги нерегульовані LDO
Стабілізатори напруги нерегульовані LDO
 Диністори
Диністори
 Діоди
Діоди
 Діоди Шотки SMD
Діоди Шотки SMD
 Діоди Шотки THT
Діоди Шотки THT
 Запобіжні діоди
Запобіжні діоди
 Діоди запобіжні SMD
Діоди запобіжні SMD
 Діоди transil SMD однонаправлені
Діоди transil SMD однонаправлені
 Діоди transil THT двонаправлені
Діоди transil THT двонаправлені
 Стабілітрони
Стабілітрони
 Стабілітрони THT
Стабілітрони THT
 Діоди інші
Діоди інші
 Комплекти пускові
Комплекти пускові
 Модулі зв'язку
Модулі зв'язку
 Модулі зв'язку RF
Модулі зв'язку RF
 Мости випрямні
Мости випрямні
 Мости однофазні
Мости однофазні
 Однофазні мости діодні SMD/THT
Однофазні мости діодні SMD/THT
 Однофазні мости діодні круглі
Однофазні мости діодні круглі
 Однофазні мости діодні плоскі
Однофазні мости діодні плоскі
 Мости трифазні
Мости трифазні
 Трифазні мости діодні
Трифазні мости діодні
 Оснащення для напівпровідників
Оснащення для напівпровідників
 Підставки DIP стандартні
Підставки DIP стандартні
 Підставки PLCC
Підставки PLCC
 Підставки прецизійні
Підставки прецизійні
 Підставки тестові
Підставки тестові
 Радіатори - оснащення
Радіатори - оснащення
 Тиристори
Тиристори
 Транзистори
Транзистори
 Транзистори NPN SMD
Транзистори NPN SMD
 Транзистори PNP SMD
Транзистори PNP SMD
 Транзистори і модулі IGBT
Транзистори і модулі IGBT
 Інструмент для паяння
Інструмент для паяння
 Інструменти для паяльних робіт
Інструменти для паяльних робіт
 Кінцівки і сопла паяльні
Кінцівки і сопла паяльні
 Паяльники нагрівальні і трансформаторні
Паяльники нагрівальні і трансформаторні
 Паяльні станції - аксесуари
Паяльні станції - аксесуари
 Стрічки випаювальні
Стрічки випаювальні
 Устаткування паяльне інше
Устаткування паяльне інше
 Флюси
Флюси
 Хімічні препарати для паяльних робіт
Хімічні препарати для паяльних робіт
 Паяльні пристрої і освітлювачі
Паяльні пристрої і освітлювачі
 Паяльні і випаювальні станції
Паяльні і випаювальні станції
 Припої паяльні
Припої паяльні
 Вимірювальні аксесуари
Вимірювальні аксесуари
 Гнізда бананові
Гнізда бананові
 Гнізда бананові 4мм
Гнізда бананові 4мм
 Зонди і насадки для виміру
Зонди і насадки для виміру
 Зубчасті затиски
Зубчасті затиски
 Затиски крокодил 4мм
Затиски крокодил 4мм
 Затиски крокодил інші
Затиски крокодил інші
 Проводи вимірювальні
Проводи вимірювальні
 Штекери бананові і вилкові
Штекери бананові і вилкові
 Штекери бананові 4мм
Штекери бананові 4мм
 Щупи - входи, виходи вимірювальні
Щупи - входи, виходи вимірювальні
 Антистатика
Антистатика
 Індивідуальний захист ESD
Індивідуальний захист ESD
 Інструменти
Інструменти
 Інструменти для зняття ізоляції
Інструменти для зняття ізоляції
 Інструменти для огляду
Інструменти для огляду
 Викрутки, настроювальні пристрої
Викрутки, настроювальні пристрої
 Затис. пристр. для након., з'єдн. і хом.
Затис. пристр. для након., з'єдн. і хом.
 Затискні пристрої для штепселів RJ
Затискні пристрої для штепселів RJ
 Затискні пристрої інші
Затискні пристрої інші
 Ключі, набори ключів
Ключі, набори ключів
 Шестигранні і зіркоподібні ключі
Шестигранні і зіркоподібні ключі
 Пінцети
Пінцети
 Пінцети ESD
Пінцети ESD
 Пінцети універсальні
Пінцети універсальні
 Пістол. для скл., устан. гаряч. повіт.
Пістол. для скл., устан. гаряч. повіт.
 Сверла
Сверла
 Щипці, ножиці, ножі
Щипці, ножиці, ножі
 Кліщі-кусачки плоскі і напівкругл
Кліщі-кусачки плоскі і напівкругл
 Кліщі-кусачки універсальні
Кліщі-кусачки універсальні
 Ножиці, маленькі ножиці, ножі
Ножиці, маленькі ножиці, ножі
 Будова прототипів
Будова прототипів
 Комплекти монтажні
Комплекти монтажні
 Ламінати мідні
Ламінати мідні
 Ламінати двосторонні
Ламінати двосторонні
 Матеріали для виробниц. друкованих плат
Матеріали для виробниц. друкованих плат
 Плати універсальні
Плати універсальні
 Вимірювальна апаратура
Вимірювальна апаратура
 Вимірники панельні
Вимірники панельні
 Вимірники панельні аналогові
Вимірники панельні аналогові
 Вимірники і приставки затискн
Вимірники і приставки затискн
 Вимірники щипцеві насадки AC
Вимірники щипцеві насадки AC
 Мультиметри цифрові
Мультиметри цифрові
 Осцилоскопи і скопометри
Осцилоскопи і скопометри
 Тестери і вимірники електричних систем
Тестери і вимірники електричних систем
 Кабелешукачі і металошукачі
Кабелешукачі і металошукачі
 Техніка складування
Техніка складування
 Контейнери і коробки
Контейнери і коробки
 Упаковка
Упаковка
 Хімічні препарати
Хімічні препарати
 Клеї
Клеї
 Маркери, фломастери, фарби
Маркери, фломастери, фарби
 Пасти термопровідні
Пасти термопровідні
 Препарати змащувальні
Препарати змащувальні
 Препарати чистячі і консервуючі
Препарати чистячі і консервуючі
 Стрічки
Стрічки
 Стрічки, що самовулканізуються
Стрічки, що самовулканізуються
 Стрічки теплопровідні
Стрічки теплопровідні
 Хімічні препарати інші
Хімічні препарати інші
 Варистор
Варистор
 Дросселі
Дросселі
 Дроселі SMD
Дроселі SMD
 Дроселі вертикальні
Дроселі вертикальні
 Дроселі кільцеві
Дроселі кільцеві
 Кварци і фільтри
Кварци і фільтри
 Кварцеві резонатори SMD
Кварцеві резонатори SMD
 Конденсатори
Конденсатори
 Конденс.низькоімпеданс
Конденс.низькоімпеданс
 Конденсатори для двигунів
Конденсатори для двигунів
 Конденсатори MLCC SMD
Конденсатори MLCC SMD
 Конденсатори MLCC SMD 1206
Конденсатори MLCC SMD 1206
 Конденсатори електр. ТНТ біполярні
Конденсатори електр. ТНТ біполярні
 Конденсатори електр. гвинтові та інші
Конденсатори електр. гвинтові та інші
 Конденсатори елкт. SMD
Конденсатори елкт. SMD
 Конденсатори керамічні
Конденсатори керамічні
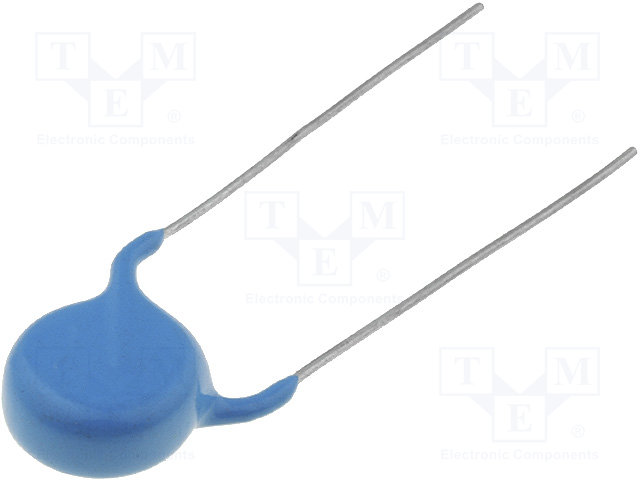 Конденсатори керамічні THT 10кВ
Конденсатори керамічні THT 10кВ
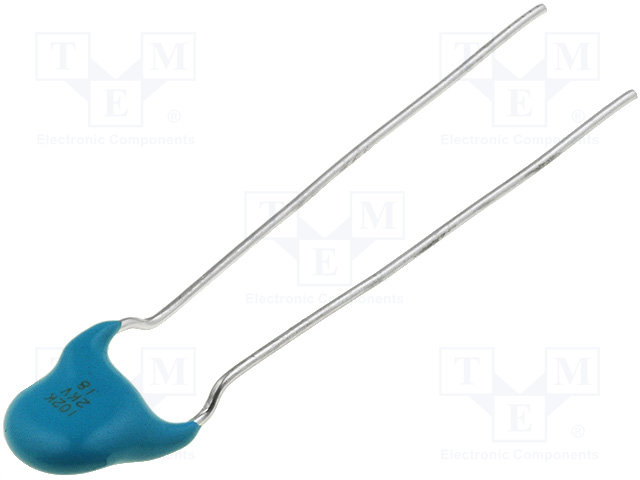 Конденсатори керамічні THT 2кВ
Конденсатори керамічні THT 2кВ
 Конденсатори керамічні THT 3кВ
Конденсатори керамічні THT 3кВ
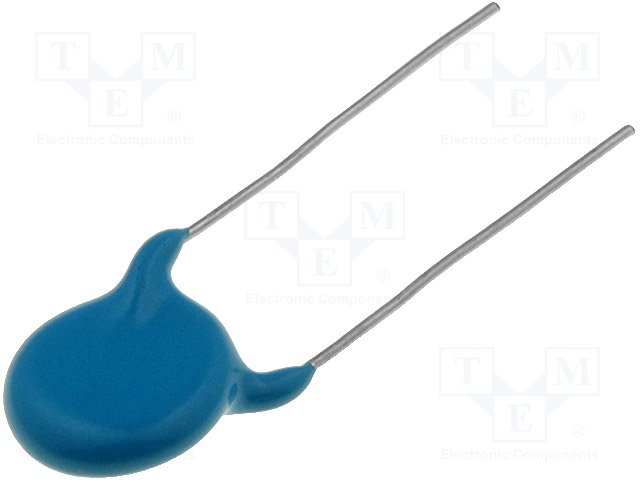 Конденсатори керамічні THT 4кВ
Конденсатори керамічні THT 4кВ
 Конденсатори керамічні THT 500В
Конденсатори керамічні THT 500В
 Конденсатори плівкові
Конденсатори плівкові
 Конденсатори полімерні
Конденсатори полімерні
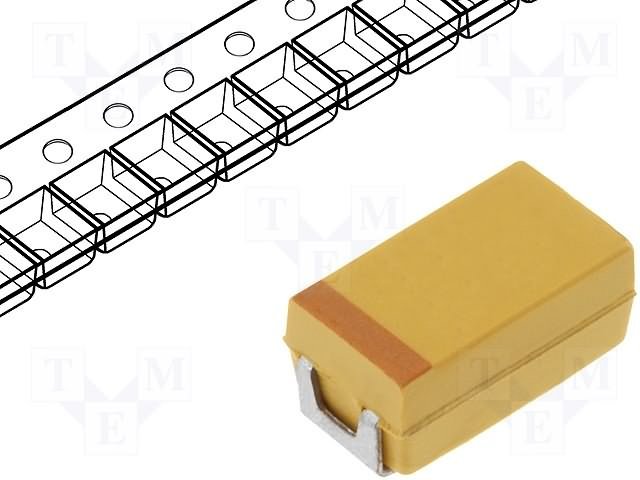 Конденсатори танталові
Конденсатори танталові
 Конденсатори танталові THT
Конденсатори танталові THT
 Конденсатори танталові SMD
Конденсатори танталові SMD
 Конденсатори MLCC THT
Конденсатори MLCC THT
 Ручки для потенціометрів
Ручки для потенціометрів
 Потенціометри
Потенціометри
 Потенціометри монтажні
Потенціометри монтажні
 Потенціометри THT багатообор. 3/8 дюйма
Потенціометри THT багатообор. 3/8 дюйма
 Потенціометри THT багатооборотні 19мм
Потенціометри THT багатооборотні 19мм
 Потенціометри багатооборотні дротяні
Потенціометри багатооборотні дротяні
 Потенціометри аксіальні однооборотні
Потенціометри аксіальні однооборотні
 Потенціометри одноообор. з пров. пласт.
Потенціометри одноообор. з пров. пласт.
 Потенціометри повзункові
Потенціометри повзункові
 Пристрої захисту від перенапруги
Пристрої захисту від перенапруги
 Резистори
Резистори
 Резистивні зборки
Резистивні зборки
 Резистори SMD 0603
Резистори SMD 0603
 Резистори SMD 1206
Резистори SMD 1206
 Резистори вугільні THT
Резистори вугільні THT
 Резистори вугільні THT 1/4Вт
Резистори вугільні THT 1/4Вт
 Резистори вугільні THT 1/8Вт
Резистори вугільні THT 1/8Вт
 Резистори металізовані THT
Резистори металізовані THT
 Резистори металізовані THT 0,4Вт
Резистори металізовані THT 0,4Вт
 Резистори металізовані THT 2Вт
Резистори металізовані THT 2Вт
 Резистори металізовані THT 3Вт
Резистори металізовані THT 3Вт
 Резистори потужності
Резистори потужності
 Резистори дротяні 10Вт
Резистори дротяні 10Вт
 Резистори дротяні 15Вт
Резистори дротяні 15Вт
 Резистори дротяні 17Вт
Резистори дротяні 17Вт
 Резистори дротяні 25Вт
Резистори дротяні 25Вт
 Резистори дротяні 2Вт
Резистори дротяні 2Вт
 Резистори дротяні 50Вт
Резистори дротяні 50Вт
 Резистори дротяні 7Вт
Резистори дротяні 7Вт
 Термістори
Термістори
 Феррит
Феррит
 Енкодери
Енкодери
 Джойстики
Джойстики
 Клавіатури
Клавіатури
 Мікроперемикачі
Мікроперемикачі
 Мікроперемикачі, TACT PCB
Мікроперемикачі, TACT PCB
 Ковпачки TACT
Ковпачки TACT
 Перемикачі ножні
Перемикачі ножні
 Перемикачі панельні
Перемикачі панельні
 Перемикачі типа Rocker
Перемикачі типа Rocker
 Перемикачі важелні
Перемикачі важелні
 Перемикачі натискові
Перемикачі натискові
 Перемикачі оборотні
Перемикачі оборотні
 Перемикачі повзункові
Перемикачі повзункові
 Перемикачі противандальні
Перемикачі противандальні
 Перемикачі типа Dip-Switch
Перемикачі типа Dip-Switch
 Свічи і замки
Свічи і замки
 Індикатори
Індикатори
 Світлодіодні контрольні лампочки
Світлодіодні контрольні лампочки
 Аксесуари для кабелів
Аксесуари для кабелів
 Виводи, ущільнювачі
Виводи, ущільнювачі
 Гайки для кабельних вводів
Гайки для кабельних вводів
 Сальники
Сальники
 Маркери проводів
Маркери проводів
 Тримачі, скоби для кабелів
Тримачі, скоби для кабелів
 Тримачі для хомутів
Тримачі для хомутів
 Кабелі
Кабелі
.jpg) Кабелі аудіо-відео
Кабелі аудіо-відео
 Кабелі акустичні
Кабелі акустичні
 Кабелі мікрофонні
Кабелі мікрофонні
 Кабелі для автомоб. обладнання FLRY
Кабелі для автомоб. обладнання FLRY
 Кабелі для передачі даних
Кабелі для передачі даних
 Телекомунікаційні кабелі
Телекомунікаційні кабелі
 Кабелі коаксиальні
Кабелі коаксиальні
 Плетінки мідні
Плетінки мідні
 Проводи багатожильні
Проводи багатожильні
 Проводи багатожильні екрановані
Проводи багатожильні екрановані
 Проводи багатожильні неекрановані
Проводи багатожильні неекрановані
 Проводи одножильні
Проводи одножильні
 Проводи одножильні - трос
Проводи одножильні - трос
 Проводи силіконові
Проводи силіконові
 Проводи силіконові багатожильні
Проводи силіконові багатожильні
 Проводи стрічкові
Проводи стрічкові
 Проводи стрічкові одноколірні
Проводи стрічкові одноколірні
 Проводи термостійкі
Проводи термостійкі
 Кабелі сполучні
Кабелі сполучні
 Кабелі аудіо-відео інші
Кабелі аудіо-відео інші
 Кабелі з перехідниками RJ45
Кабелі з перехідниками RJ45
 Кабелі сполучні коаксиальні
Кабелі сполучні коаксиальні
 Кабелі сполучні телефонні
Кабелі сполучні телефонні
 Кабелі і адаптери HDMI, DVI, DisplayPort
Кабелі і адаптери HDMI, DVI, DisplayPort
.jpg) Кабелі і адаптери USB
Кабелі і адаптери USB
 Кабелі і адаптери для моніторів
Кабелі і адаптери для моніторів
 Комп'ютерні кабелі і адаптери
Комп'ютерні кабелі і адаптери
 Комутаційні кабелі і оптичні пигтейли
Комутаційні кабелі і оптичні пигтейли
 Сполучні кабелі живлення
Сполучні кабелі живлення
 Кабелі живлення DC
Кабелі живлення DC
 Кабелі живлення комп'ютерні і універс.
Кабелі живлення комп'ютерні і універс.
 Обплетення і захисні оболонки
Обплетення і захисні оболонки
 Трубки термозбіжні
Трубки термозбіжні
 Контактори
Контактори
 Реле
Реле
 Реле електромагнітні
Реле електромагнітні
 Реле електромагнітні - аксесуари
Реле електромагнітні - аксесуари
 Реле електромагнітні автомобільні
Реле електромагнітні автомобільні
 Реле електромагнітні високотокові
Реле електромагнітні високотокові
 Реле електромагнітні герконові
Реле електромагнітні герконові
 Реле електромагнітні мініатюрні
Реле електромагнітні мініатюрні
 Реле електромагнітні промислові
Реле електромагнітні промислові
 Реле напівпровідникові
Реле напівпровідникові
 Реле SSR однофазні
Реле SSR однофазні
 Реле SSR постійного струму
Реле SSR постійного струму
 Мікродвигуни і аксесуари
Мікродвигуни і аксесуари
 Трансформатор струму
Трансформатор струму
 Трансформатори для друку
Трансформатори для друку
 Трансформатори з кріпленням
Трансформатори з кріпленням



